

Recherche des actifs végétaux pour des cultures d’essai et de contrôle appliquées à l’artemisia annua
Le paludisme est une des maladies parasitaires les plus importantes dans le monde. Chaque année, environ 500 millions de personnes sont touchées par le parasite, et parmi eux, 90% vivent en Afrique sub-saharienne, où le paludisme est la principale cause de décès.
L’augmentation de la mortalité ces dernières années est liée à la propagation de Plasmodium falciparum transmis par Anopheles résistante aux courants et peu coûteux médicaments antipaludiques tels que la chloroquine et la sulfadoxine-pyriméthamine.
La nécessité pour les pays en voie de développement ont, tout d’abord, de compter sur les outils de développement inhérentes au territoire, pour encourager la mise en valeur des espèces végétales qui sont inclus dans les médecines naturelles ou sont compatibles avec des aléas climatiques et géo-culturelle.
Le choix d’encourager la culture d’Artemisia annua au Burundi, comme projet pilote, a été réalisé principalement en tenant compte de la facilité de culture et d’élevage, et des caractéristiques de la culture agricole du pays.
Historie du projet
Le projet est né en 2005 ; il a eu pour but précis, pour la première année de sa mise en œuvre, la expérimentation de la culture dans différentes régions du Burundi, de l’herbe Artemisia annua. Cette plante, d’origine orientale (Chine, Cambodge, Vietnam) contient l’artémisinine, l’ingrédient actif efficace contre les souches de Plasmodium falciparum résistantes à la quinine, l’agent causal du paludisme.
En 2006, s’est poursuivi avec l’identification de domaines supplémentaires qui conviennent pour la culture d’Artemisia annua.
En 2007, le F.I.M.A.C. a élaboré un protocole d’entente avec le ministère de la Santé du Burundi, destiné à l’étude des plantes médicinales, et une collaboration entre les chercheurs du Département de biologie de base, Département de sciences de l’environnement et de chimie appliquée et génie de l’Université de ‘Aquila pour l’analyse des principes actifs, pour le développement de méthodes appropriées pour le pays, pour l’optimisation et l’augmente du contenu de l’artémisinine dans les plantes in vitro et in vivo.
En 2009, l’association italo / A.Da.Spes Burundi (Association pour le developpement Spes – Bujumbura – Burundi) deviens partner de le projet comme co-ordinator des activités sur place et la diffusion de la santé des cultures.
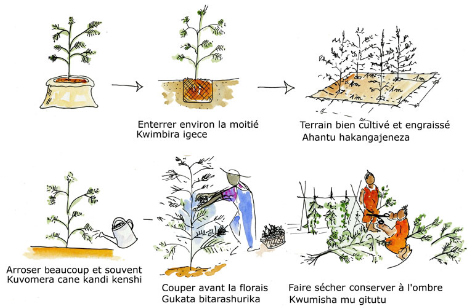 Informations techniques
Informations techniques
L’artémisinine est une lactone sesquiterpène avec un anneau triossanic comportant une liaison peroxy, qui est essentiellement liée à l’activité antipaludique.
La voie de biosynthèse de l’artémisinine dans la plante suit le chemin de l’acide mévalonique et de farnesilpirofosfato, qui successivement ciclize par une adénylate terpène.
Pour un but pharmaceutique le cétone en 10 concentrations de l’artémisinine peut être hydrogéné pour former la dihydroartémisinine hémiacétal, qui en outre transformé en dérivé donne naissance à des composés solubles dans l’eau tels que l’artésunate, sel de sodium d’ester succinique, ou l’artéméther ester lipophile.
Depuis l’artémisinine et ses dérivés agissent très rapidement sur le parasite, mais sont tout aussi rapidement éliminé de l’organisme, sont administrés combinaisons basées sur des dérivés semi-synthétiques de ‘artémisinine (ACT – nouvelles associations thérapeutiques à base d’artémisinine) que l’artéméther, artésunate et artemisone , et un autre médicament antipaludique, tels sulfametossipirazina, pyriméthamine ou pipéraquine, qui persiste plus longtemps dans l’organisme, en garantissant l’élimination complète de toute trace de l’infection.
La préparation de la perfusion fournit certaines mesures telles que l’utilisation de l’eau très chaude (environ 90 ° C), mais pas bouillante, car bouillir les feuilles dans de l’eau cause la dégradation de l’artémisinine, alors que dans les solvants neutres artémisinine est stable jusqu’à à 150 ° C.
Il faut rappeler que l’eau doit être en bonne proportion, de manière à assurer l’extraction complète du principe actif (5 à 10 gr.foglie séchées pour 1 litre d’eau, pour les plantes qui contiennent jusqu’à 1, 5% l’artémisinine).
Le mécanisme d’action de l’artémisinine est exprimée en interférant dans le transport de la membrane et dans le bloc de fonction mitochondriale du parasite, encore, elle module le système immunitaire de l’hôte et inhibe l’angiogenèse. L’élément clé est due à l’inhibition d’une enzyme du parasite membre du transport membranaire (sarcoplasmique réticulum endoplasmique-ATPase-SERCA) de calcium, et il est la perturbation de l’homéostasie du calcium qui causes de la mort du parasite ; donc, le possible développement d’une résistance au parasite pourrait être associé à la surproduction ou la mutation de ce transporteur.
Chef de projet: Dr. Paolo Monti
Coordinateur Scientifique: Dr. Giordana Marcozzi
| Participants italiens: | Établissement Département: |
| Dr. Paolo Monti | FIMAC Roma |
| Dr. Giordana Marcozzi | Dip. Biologia di Base Applicata – Università di L’Aquila |
| Dr. Loretta Pace | Dip. Scienze Ambientali – Università di L’Aquila |
| Dr. Samantha Reale | Dip. Chimica e Ingegneria dei Materiali – Università di L’Aquila |
| Dr. Antonella Angelosante | Dip. Scienze Ambientali – Università di L’Aquila |
| Prof. Laura Spanò | Dip. Biologia di Base Applicata – Università di L’Aquila |
| Prof. Francesco De Angelis | Dip. Chimica e Ingegneria dei Materiali – Università di L’Aquila |
| Dr. Alessandra Macri | Consulente internazionale in cooperazione e sviluppo |
| Participants du Burundi: | Établissement Département: |
| Dr. Albert Mbonerane | ALUMA (Association de Lutte Contre la Malaria) – Bujumbura |
| Sig. Ottavio Framarin | A.DE.SPES – Bujumbura |
Bibliographie
Chang HM., But PPH. Pharmacology and applications of Chinese Materia Medica; Vol.1, Singapore: World Scientific Publishing (1986).
www.msf.it/editoriale/220405.shtml
Greewood B., Mutabingwa T., Nature 415 (2002) 670.
www.anamed.net/
Chunzhao Liu, Yan Zhao, Yuchun Wang Artemisinin: current state and perspectives for biotechnological production of an antimalarial drug. Appl Microbiol Biotechnol 72:11 (2006).
Paniego B. et al. Medicinal and Aromatic Plants in Biotechnology in agriculture and Forestry, Vol.24, p.64 (1994).
Ferreira J.F.S. Distribution of artemisnin in Artemisia annua. In Progress in new crops. ASHS Press, Arlington, VA, 1996.
Van Nieuwerburg et al. J Chromat.A 2006.
Hsu E. The history of qing hao in the Chinese materia medica. Ts Roy Soc Trop Med Hyg 100:285 (2006).
Alfonso A. et al. Malaria parasites can develop esistance to Artemisinin.. Antimicr. Agents Chemotheraphy 50:480 (2006).
Rath et al., Am J. Trop. Med. Hyg. 2004.
Willcox ML. Et al.. Artemisia annua as a traditional herbal antimalarial. In Willcox ML, Bodeker G and Rasoanaivo P. (2004). Traditional Medicinal Plants and malaria. Boca Raton: CRC Press.
World Health Organization. The use of antimalarian Drugs. Geneva. WHO/CDS/RBM/33 (2001).
Liang P.H. et al ism and function of prenyltransferases. Eur J Biochem 279: 3339 (2002).
Julsinf M.K. et al Combinatorial biosynthesis of medicinal plant secondary metabolites. Biomecular Engineering 23:265 (2006).
Ramharter M. Et al In vitro activity of artemisone compared with artesunate against Plasmodium falciparum. Am J Trop Med Hyg. 75: 637 (2006).
Sagara I et al. A randomized trial of artesunate-pyrimethamine versus artemether-lumefantrine for the treatment of uncomplicate Plasmodium falciparum malaria in Mali. Am J Trop Med Hyg. 75: 630 (2006).
Edlund et al. Acta Pharm Suec., 1984.
Christen and Veuthey Curr. Med. Chem. 2001.
Becke K and Kirk K. Of malaria, metabolism and membrane transport. Trends in Parasitol. 20, 509 (2004).
Golenser J. et al. Current perspectives on the mechanism of action of artemisinina. Intern. J. Parasitol. 36, 1427-41, 2006.
Naik H. et al J Chromat. B 2005.
Zhao and Zeng, Planta Med. 1985.
Zhao, Analist, 1987.
Xing et al. Rapid Comm. Mass Spectrom. 2007.
Klayman et al. 1984.
Chenfei M. et al. Analysis for Artemisia annua L. volatile oil by comprehensive two dimensional gas chromatography time-of-flight mass spectrometry. J Chrom. A, 1150: 50 (2007).
Monti P. Relazione FIMA, marzo 2006.
_________________________________________
Samantha Reale 1, Loretta Pace 2, Paolo Monti 3, Francesco De Angelis 1 and Giordana Marcozzi 4*
1 Dept. Chemistry and Chemical Engine and Material, University of L’Aquila
2 Dept. Environmental Sciences, University of L’Aquila
3 F.I.M.A.C. Onlus (Italian Doctor Foundation for Central Africa), Piazza Montevecchio, 22 – 00186 Rome, Italy
4 Dept Basic and Applied Biology, University of L’Aquila, Via Vetoio, 67010 AQ – Italy
Samantha Reale 1, Loretta Pace 2, Paolo Monti 3 and Giordana Marcozzi 4*
* Dept. Basic and Applied Biology, University of L’Aquila, Via Vetoio, 67010 AQ – Italy
Telephone +39.0862.43.3244, fax +39.0862.43.3273
e-mail: giordanamarcozzi@hotmail.com
info@fimaconlus.it
Abstract
We describe a simple, rapid combined method for extracting the antimalarial compound artemisinin from the leaves of Artemisia annua, L. cultivated for the first time in Burundi, and quantitating the active principle by high-performance liquid chromatography-electrospray mass spectrometry (HPLC-ESIMS).
